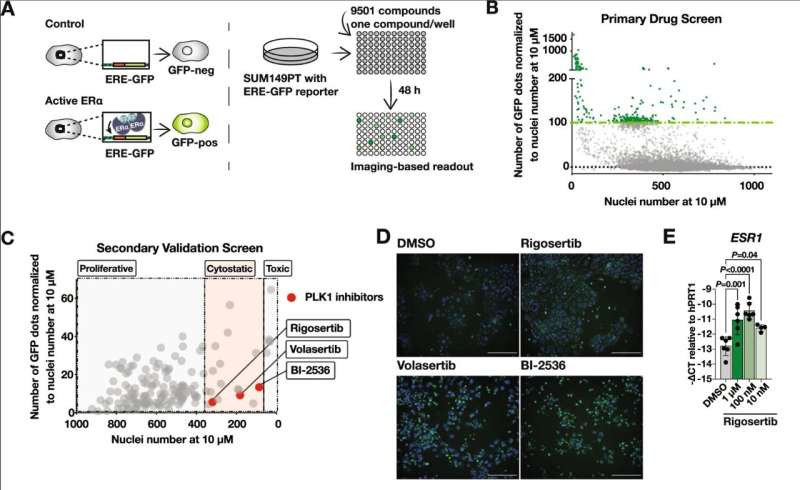
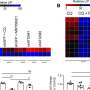
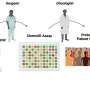
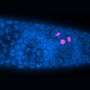
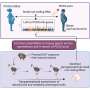
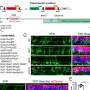
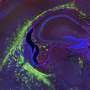
高通量药物筛选揭示雌激素受体α(ERα)感应在三阴乳腺癌(TNBC) polo-like激酶1 (PLK1)抑制。高通量药物筛选的原理来确定抑制剂诱导ERαTNBC的信号。ERα信号不表达GFP细胞不活跃,而细胞活跃ERα信号触发ERE-GFP记者和表达绿色荧光蛋白。化合物增加了48 h SUM149PT ERE-GFP细胞。GFP信号和赫斯特与荧光显微镜测定活细胞的信号。B点情节描绘GFP信号和核数来自赫斯特染色从屏幕的主要药物。C点情节描绘GFP信号和核数来自赫斯特染色从次要验证屏幕。每个点代表的意思是三个技术复制。点击分为增殖,抑制细胞生长的或有毒的。PLK1抑制剂在红色的描述。 D Representative fluorescence microscopy live-cell images from the validation screen shown in Fig. 1C. SUM149PT cells were treated with the indicated PLK1 inhibitors for 48 h. The ERE-GFP signal is depicted in green, the Hoechst nuclei stain in blue. Scale bars: 100 µm. E Immunoblot showing levels of ERα and ERK2 (loading control) in SUM149PT cells treated for 72 h with rigosertib or DMSO at the indicated concentrations. Credit:致癌基因(2022)。DOI: 10.1038 / s41388 - 022 - 02429 - 0
癌症发生在细胞体内肆意地生长和扩散到其他器官。癌细胞在许多方面不同于正常细胞。癌细胞的特点之一是其高适应性体内不同的环境和药物治疗。在这个特点,他们像干细胞或细胞在成熟的早期阶段。
巴塞尔大学的研究人员和巴塞尔大学医院测试的可能性人为到期(或者更准确地说,区分)乳腺癌细胞作为一个方法来把它们变成更正常的细胞类型。
分化是一个治疗策略血源性癌症治疗已成功实现,但是没有在实体肿瘤。在《致癌基因,现在教授Mohamed Bentires-Alj领导一个研究小组报道有前途的新结果。研究人员能够使用分化治疗一个特别强势的类型称为三阴性乳腺癌的癌。
“我们展示在这里,我们可以将乳腺癌细胞转化为更少的有害的细胞停止生长,“说Bentires-Alj谁是组长的生物医学。
双重雌激素受体的活动
雌激素作为信号分子在细胞通过绑定到其同源受体,雌激素受体,从而诱导一系列生物效应。在正常乳腺细胞表达雌激素受体是成熟的专业乳腺细胞和不扩散。
相反,在一小部分乳腺癌细胞表达雌激素受体明显增多。调用这些乳腺癌雌激素受体阳性乳腺癌和包括所有乳腺癌病例的75%左右。因为他们容易受到雌激素,可使用反雌激素疗法,治疗非常有效的病人。
的三阴性乳腺癌然而,子类型是不容易受到雌激素或抗雌激素。这种类型的癌主要发生在绝经前妇女,往往缺乏有效的治疗方法。“我们最初的想法是引起雌激素受体的表达,以雌性激素受体阳性乳腺癌三阴性乳腺癌转换成因为这个亚型可用的更有效的治疗方案,”博士说,这项研究的首席作者Milica Vulin。
与诺华公司合作,研究小组测试了超过9500种化合物的功效达到这一目标。他们发现,最有前途的化合物显示结果称为polo-like的必不可少的细胞周期蛋白激酶抑制剂1 (PLK1)。抑制这种蛋白质导致所需增加的表达雌激素受体。研究人员吃惊的是,这并不只是将三阴性乳腺癌细胞转换成一种更易于管理癌症细胞。它转换他们的细胞类似于正常细胞。
影响治疗
”细胞和理解分子机制定义不同于癌症和如何将这些机制正常细胞开发新的创新疗法至关重要,“Bentires-Alj说。结果治疗三阴乳腺癌的研究开辟新途径。“这项研究中使用的化合物已经在临床试验治疗其他癌症类型,包括血源性、肺、和胰腺癌”,研究人员仍在继续。这突显出的可能性在诊所和测试这些化合物在治疗乳腺癌。
特别是在时代的免疫疗法,有人建议,细胞可以通过“常规”免疫系统而“癌”细胞逃避免疫细胞死亡。在未来,仍有待决定如果分化疗法可以结合免疫疗法。“我们追求这些策略,只有时间和资源在我们取得进一步进展,”研究人员总结道。
更多信息:Milica Vulin et al,高通量药物屏幕显示方式区分三阴性乳腺癌,致癌基因(2022)。DOI: 10.1038 / s41388 - 022 - 02429 - 0
期刊信息:致癌基因
所提供的巴塞尔大学