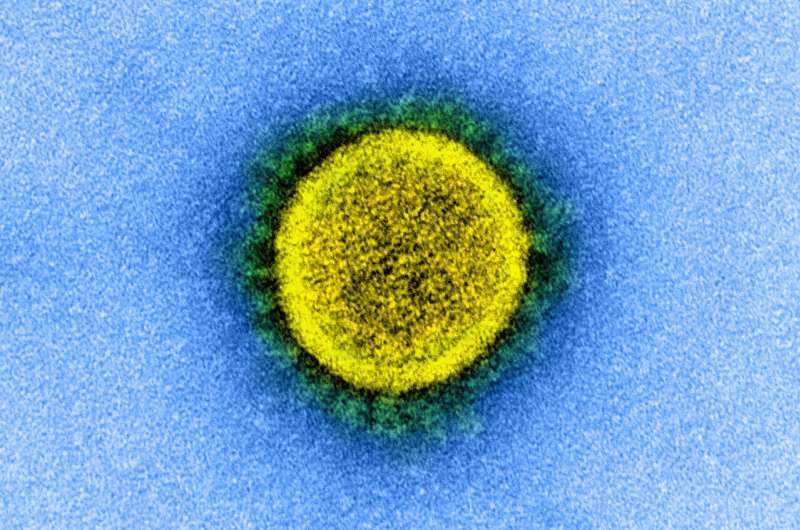
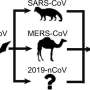
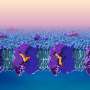
SARS-CoV-2在电子显微镜图像(如图所示)。来源:国家过敏症和传染病研究所,国家卫生研究院
花了冠状病毒,科学家最终问题的伦理标准安慰剂对照研究。甚至最主流科学期刊,如自然,现在终于终于承认,没有人应该把他们年迈的父母,孩子或必要的同事在对这种病毒注入假。
坦率地说,这是一个惊人的背离官方叙事医学的双盲安慰剂对照试验成本。科学又说,看起来,它说,大型制药公司可以保持他们的安慰剂。相反,那些愿意勇敢的新疫苗可以参加更合适的生物标志物的研究,每个人都得救。可见在这些研究不仅仅是屈服还是生存,而是这抗体和保护你自己独特的防御系统安装或失败。可以想象其他的医学不是太远。
但如果疫苗不能跟上所有的新变种,例如,E484K变体首先指出在南非,现在阻挠试图控制传播?就此而言,这些新病毒是如何传播?他们是一次性事件,然后成立飞在原产地从遥远的国家,或者是这些multiregional突变,产生新创在当地居民吗?更重要的是,第一个病毒是从哪里来的?
仍有很多不确定性关于非典的起源,但有一件事我们可以自信来讲弱智傻子让另一个人告诉他们什么是真实的信息,什么是错误的。非典的真相在健康的头脑,和其他复杂问题上,从来都不是没有强加的东西;它必须通过经验中我们每个人都到达。最近的一个众所周知的纸生态学与进化的趋势题为“解开SARS-CoV-2的人畜共患的起源和传播”,由于其标题,似乎有特殊的冠状病毒的事实。
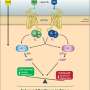
作者指出,一些蝙蝠困难冠状病毒,如RaTG13序列,含有高达96.2%的序列与SARS-CoV-2身份。这种病毒可能因此成为我们的来源,也可能只是并行进化。在2002 - 2003年非典(SARS)爆发,可能人畜共患来源是果子狸(Paguma larvata),进行SARS病毒有99.8%相同的序列的病毒爆发。作者继续描述病毒感染穿山甲,所谓的中间宿主,具有耐人寻味的相似之处SARS-CoV-2关键ACE2的受体结合区域的峰值蛋白质。有趣,虽然在公平穿山甲,在全基因组水平,这些病毒只有85.5 - -92.4% SARS-CoV-2相似。因此,他们需要很大程度的自然进化或实验室使演变成我们现在面对的病毒。
面对环境的不确定性,但好奇的人平均要么自己成为一个专家,或者找专家他们信任。换句话说,他们应该确定足够的勇气来反抗怀疑官方的叙述当缺陷被发现。当搜索这样的学习个体在数字以太,新的信息关于这个anti-pangolin光纸。Twitter用户@WackyScience指出细胞纸依赖于自然纸上寻找灵感这些穿山甲的事情,一个重要的齿顶高静静地一直下滑。即,穿山甲的样本受到了污染与人类和老鼠的材料。对于那些想深入,@NoWackyScience提供了一些巧妙地编译动机链接:
上面最后一个条目是由一位杰出博士后Broad研究所的成员,陈爱丽娜,阐明造成了其他人一样越来越神秘的起源RaTG13序列。似乎有更多比最初的故事。陈抱歉到达她的结论对于中国公布的恶作剧RaTG13序列。她说只是因为这种“阴谋论”的起源可以真正的在她看来,这些病毒序列其他阴谋论在其他主题仍然是毫无根据的。然而,她说,说有可能是病毒的实验室不是阴谋论;它仅仅是一个理论。逃脱事件是一个真正的现象,他们最近历史上发生过很多次,这不可思议的想象在那些我们认为我们的生化武器实验室基金更宽松的外国黄土运作的方式。
而这当然是可能的,甚至有可能,所有独特的转换冠状病毒使其前所未有的传染性自然进化在其它种类的动物和无缝地冲破障碍我们(换句话说,完全是人畜共患),其他逻辑解释的观测数据确实存在。其他解释,像逃离实验室,专门从事病毒功能转换,正在看着更密切地在几个主流场馆。在这一点上,重要的是要注意,官方媒体在事实上,现有的科学在病毒起源是叙事,它不可能是一个逃脱。
一个炸弹的故事出现的一天纽约杂志,让许多资金雄厚传染病实验室负责人的心漏跳一拍。Nicholson Baker,作者是一名小说家和散文家而非传染病病毒学家。然而,他却不知怎么文档我们现状的事实明显比专家更彻底和简洁。一些深入了解为什么这是今天可能可以通过考虑科学知识的过程现在打包给公众。甚至今天,科学家和科学作家经常谈话要点,直接或间接,如何向公众介绍科学知识。换句话说,不仅指导科学应该被认为是造谣,还如何正确应对某些所谓的造谣。
例如,一个受人尊敬的学术科学家小组已经组装的所谓的“COVID-19沟通手册”来指示如何处理疫苗conspiracists。即如何应对别人问的逻辑问题,疫苗可能会成功地对抗病毒变异。简而言之,出版强烈谴责他们所谓的“疫苗行为”,与自己的目标背道而驰。奇怪的是,许多人似乎也表现出这些疫苗不良行为问题的官方叙述“非典”的起源。
也许唯一明确证明蝙蝠病毒在中国洞穴自然突变和运输本身1000英里到武汉爆发站点,这世界上最资助和先进的实验室将uninfectious SARS病毒转化为使SARS变异没有涉及到,是我们现有的知识领域的个人DNA和RNA序列变异和变换。
这是我们已经了解得非常好。换句话说,哪些特定基地自然倾向于随时间进展到其他特定的基地,通过自然过程。我们也有一个相当不错的序列是由各种DNA修复机制在更高级的生物,以及突变往往看似执导,或有偏见的在某些情况下,根据生物或主机的状态。在文献中,这些过程称为基地过渡,经常表达的最大似然估计的动态景观基础替换。
他们一般有两种类型:转换交换的two-ring嘌呤(g)和纽约市的嘧啶(C-T),虽然颠换交换的嘌呤嘧啶基地。总之,我们有16个可能的替代方案类型,每个都有独立的可能。在人类线粒体DNA,例如,我们知道过渡到颠换比例非常高。线粒体和核DNA竞争访问核苷酸的复制、转录和修复、细胞中的每个核苷酸的相对丰度影响的结果看似不同的随机事件。同样的逻辑也适用于病毒序列进化。的时机已经成熟,开始做这种类型的分析SARS的进化序列我们从动物或病人获得。
更多信息:Banerjee Arinjay et al .解开SARS-CoV-2的人畜共患的起源和传播,生态学与进化的趋势(2020)。DOI: 10.1016 / j.tree.2020.12.002
©2021科学欧宝app网彩X网络