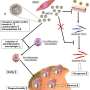
一种新的埃博拉疫苗方案正在马里兰州银泉的临床试验中心进行测试
沃尔特芦苇陆军研究院(Wrast)今天宣布启动2期临床试验,以评估患有健康和艾滋病毒感染的学习志愿者的素质增强埃博拉疫苗方案的安全性和免疫原性。
这项研究包括两个候选疫苗,来自Crucell Holland B.Z2的Ad26.Zebov.,Johnson&Johnson的Janssen制药公司之一,以及来自巴伐利亚北欧的MVA-BN-FILO,将被顺序地作为“普通增强”方案给出。七十五志愿者将接受主要剂量的MVA-BN-Filo,然后增加Ad26。明年年初,wirr在非洲的附属站点也将开始评估这种方案,以及从Ad26开始的疫苗接种计划。ZEBOV,然后加了MVA-BN-Filo。
研究人员将评估疫苗计划的安全性和耐受性以及免疫反应的特征,这将有助于他们更好地理解这些不同的方案。Janssen和其他开发合作伙伴已经从一小群健康受试者中获得了初步数据,表明两种方案都是安全的和免疫原性的。
这项研究将加强安全性和免疫原性该方案在健康受试者中的证据,并将1期研究的人群扩大到包括70岁以上的志愿者和稳定抑制hiv感染的志愿者。
“至关重要的是,我们要知道这些疫苗在将在非洲使用的社区是安全的和具有免疫原性的,”美国军方艾滋病毒研究项目(MHRP)首席副主任和这项国际研究的方案主席、传染病医生Julie Ake中校说。
该研究包括艾滋病毒感染的志愿者,因为它们代表了其中一些可能受益于非洲预防性埃博拉疫苗的人。“鉴于这两个病毒都可以出现在同一社区中,这是一个重要的考虑因素,”纳尔斯·迈克尔,MHRP主任。
该临床试验是WRAIR和詹森制药公司之一的Crucell Holland b.v.之间的合作,资金来自于国防部化学和生物防御联合项目执行办公室的联合疫苗采购计划。
这项研究最初是在马里兰州银泉的WRAIR进行的,2016年初将扩展到非洲的6个地点。总共约有575名志愿者参与。它将在与WRAIR的军事艾滋病研究项目在尼日利亚、乌干达、肯尼亚、坦桑尼亚和莫桑比克的临床研究地点进行。
这是WRAIR进行的第二项埃博拉疫苗临床试验,也将是第四项埃博拉疫苗临床试验疫苗在非洲进行的研究。
WRAIR行动副指挥官斯蒂芬·托马斯上校说:“埃博拉等传染性疾病对美国军队和全球社会构成重大威胁。”“WRAIR在传染病方面拥有广泛的专业知识,在疾病流行的国家有一个国际研究网络,这给我们提供了进行这类研究的理想平台。”
由美国军事艾滋病毒研究计划(MHRP)提供