tRNA-derived碎片的甲基化调节基因沉默在膀胱癌的活动
Anindya Dutta面交博士和他的同事描述了一种新颖的改变在膀胱癌的基因调控,导致增加的基因通路,帮助癌细胞生存在快速增长。
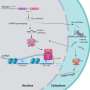
他们的工作集中在一个22-base转移rna片段称为tRF-3b,由复杂的酶称为TRMT6/61A修改。在膀胱癌TRMT6/61A-a甲基转移酶酶的水平,增加了甲基上的第四基地tRF-3bs-are升高。这一修改防止tRF-3bs压制不同的表达基因在展开的蛋白质反应的途径癌症细胞,导致这些基因的表达增加。
”我们所知,这是第一个例子,microRNA-like调控的基因沉默TRMT6/61基于N1-methyladenosine修改,我们的报告提供了一种机制,通过这种机制TRMT6/61A在癌症的高度会影响基因的表达,”杜塔说。“快速增殖的癌细胞合成和细胞比正常情况下更多的蛋白质折叠,因此需要移植的蛋白质反应途径来维持体内平衡。我们发现膀胱的一种方式癌症细胞激活pro-survival展开蛋白质反应减轻内质网压力是通过阻止扶轮基金会沉默基因的表达在这展开的蛋白质反应。”
“展开的蛋白质反应与癌症发展的许多方面紧密相连,成为一个有前途的治疗目标,”杜塔说。“这是此前指出,全球展开的蛋白质与响应相关的基因调节在多种癌症类型,包括膀胱癌,因此我们的研究结果表明,抑制TRMT6/61A酶可能是一个新的方法来治疗膀胱癌。”
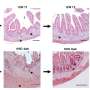
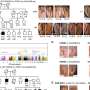
这项研究由杜塔和共同通讯作者符文Ougland医学博士博士,包括分析膀胱癌组织获得患者行经尿道膀胱肿瘤的切除。这是发表在《华尔街日报》自然通讯。Dutta椅子的伯明翰阿拉巴马大学遗传学系和Ougland泌尿道的外科医生和高级研究研究员奥斯陆大学医院Rikshospitalet,奥斯陆,挪威。
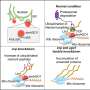
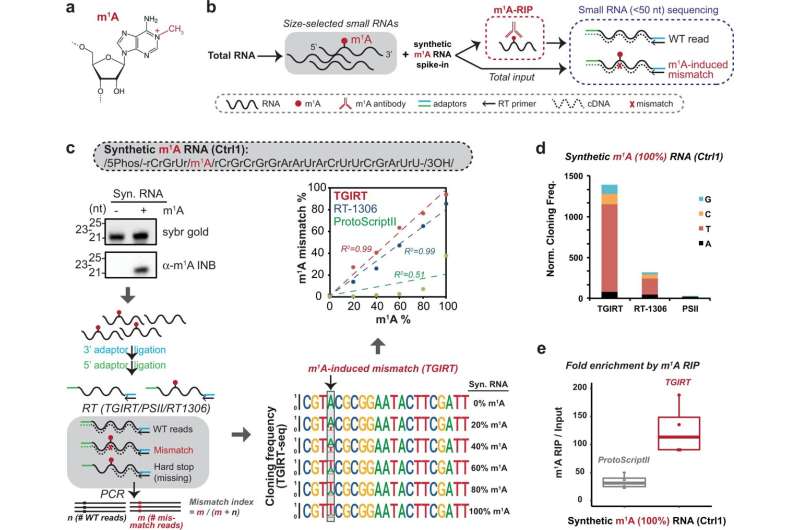
研究的一个重要进展是工作流用于创建一个图书馆从人类细胞的小分子rna N1-methyladenosine修改,或者m1答:工作流结合两个独立approaches-enrichment由m1A-antibody,紧随其后的是小RNA-sequencing和m1测序A-induced签名不匹配。
UAB研究人员发现一种逆转录酶的酶,ProtoScriptII,简称为常用的RNA序列,并很好地检测小分子RNA含有m1一个;但是另外两个反转录酶的使用工作流显示tRNA-derived片段,其中包括tRF-3b短rna中丰富。这表明小分子rna m1大多数小型rna序列库修改比例偏低,通常使用ProtoScriptII。
改进工作流程,研究人员发现,m1修改存在的主要是扶轮基金会之间的人类小rna。他们还发现,m1修改是非常具体和普遍nuclear-encoded扶轮基金会和mitochondria-encoded扶轮基金会,和m1从nuclear-encoded tRF-3b trna上发现一个是由TRMT6/61A复杂。
如何米1A-tRF-3b阻碍基因沉默吗?答案涉及到一个更深的深入分子遗传学但关键似乎是,N1-methyladenosine修改破坏常规的沃森克里克碱基配对。
小分子核糖核酸已知沉默基因通过绑定到RNA-induced沉默复杂,或RISC。他们作为一个模板来绑定互补的信使RNA,然后信使RNA沉默和RISC退化。类似于小分子核糖核酸,tRF-3s被发现在不同的生物通路,特别是基因沉默途径依赖之间的碱基配对的小分子rna,在这种情况下tRF-3s,目标rna。
研究人员创建了一个荧光素酶报告实验,发现未经修改的tRF-3引发基因沉默,而m1修改tRF-3b废除了基因沉默。“既然米1中断规范化碱基配对,我们假设m的削弱碱基配对1在tRF-3目标信使RNA基因沉默的活性降低观察米解释说1包含tRF-3s,”杜塔说。
合作者与Dutta Ougland在这项研究中,“TRMT6/61A-dependent基地tRNA-derived碎片的甲基化调节基因沉默活动和膀胱癌的展开的蛋白质反应,”苏张立敬上,阿拉巴马大学的遗传学部门;Ida Monshaugen Arne Klungland,奥斯陆大学医院Rikshospitalet;并对此威尔逊和Fengbin Wang弗吉尼亚大学。
更多信息:张立敬上苏et al, TRMT6/61A-dependent基地tRNA-derived碎片的甲基化调节基因沉默活动和膀胱癌的展开的蛋白质反应,自然通讯(2022)。DOI: 10.1038 / s41467 - 022 - 29790 - 8