在轨道上停止肠道细菌
肠子在我们身体中最多的免疫细胞。由于肠道不断地暴露于细菌和食物等各种抗原,因此肠道免疫细胞的适当诱导在肠道稳态中起着枢轴作用。
由博士联盟教授领导的Postech Research团队领导。候选人Sookjin月亮和研究助理教授云吉公园的生命科学部 - 已经揭开了第一个调节T细胞(上皮细胞,IEL)的分化的机制肠上皮细胞(IEC)。这些发现最近发表在了实验医学杂志(JEM),关于今年庆祝其125周年的免疫学杂志的权威杂志。
其位于上皮内的IEL是抵抗眼部外部在上皮细胞层中的细胞。换句话说,IEL是免疫细胞位于我们身体的周边,当遇到相比微生物等细菌时调节免疫反应。因此,IEL的适当分化对于调节肠免疫稳态至关重要。然而,IEL在IEC层内区分的确切机制很差。
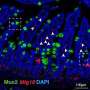
为此,研究团队在小型的远端部分寻找特定的环境因素肠由于IEL在器官的那部分中富集。通过仔细检查,IECS表达了在小肠远端部分中的微生物群诱导的主要组织相容性复合体II(MHC II)和死亡 - 配体1(PD-L1),其中CD4 + T细胞转化进入IEL。
通过这些分子,通过提供抗原特异性T细胞受体(TCR)刺激和编程的细胞死亡蛋白1(PD-1)信号传导,IECS诱导将IEC层进入IEL的T细胞的成熟。特别地,通过抑制CD4 + T细胞的母系转录调节剂的表达,PD-1信号传导诱导CD4 + T细胞的分化为IEL,这是从未报道的PD-1信号传导的新作用。
本研究表明,TCR刺激和来自常规免疫学教科书中引入的专业抗原呈递细胞(APCS)-A概念的TCR刺激和共刺激诱导的T细胞分化也可以由组织细胞诱导,而不仅仅是通过APC诱导。即使在小肠内,IECS的分子表达表明区域差异由于共生微生物等环境因素,其在其近端和远端部分之间,这表明这在每个区域的免疫细胞调节中起重要作用小肠。
“IECS通过创建CD4 + IEL抑制肠道细菌的方式并将它们放入上皮细胞层类似于培训特殊代理并将其部署到战场,”Seung-Woo Lee教授解释说。他补充说:“IECs发生的T细胞分化的事实不仅适用于肠道,而且还适用于我们身体的大多数组织,这是研究组织作用的有希望的迹象细胞。“
进一步探索











用户评论